GRAS(Generally Recognized As Safe)意為公認為安全,如果某種物質在預期用途下公認為安全,屬于GRAS,則該物質可豁免美國法律要求的上市前審批程序。作為食品新成分在美國獲得認可的重要依據,FDA GRAS申報火熱依舊。在歷經近3個月未更新之后,FDA于近日對FDA GRAS清單進行了大批量更新,目前最近更新時間為2025年6月10日。
瑞旭集團對2025年1月-2025年6月FDA GRAS物質申報情況進行了詳細的統計和匯總,供企業了解及參考。
1.2025年上半年FDA GRAS申報更新提交和通過匯總
FDA官網中,GRAS卷宗的狀態分為三類:①FDA has no questions(FDA無疑問;② Pending(等待中,即在審狀態) 和③ At the notifier's request, FDA ceased to evaluate this notice(應通知人的要求,FDA停止對該通知的評估,即申請人撤回)。
在2025年1月-2025年6月的更新中,共59款物質有狀態更新,其中,34款物質通過認證,更新了“FDA has no questions”狀態,新增15款在審物質,另有10款物質進行了撤回。
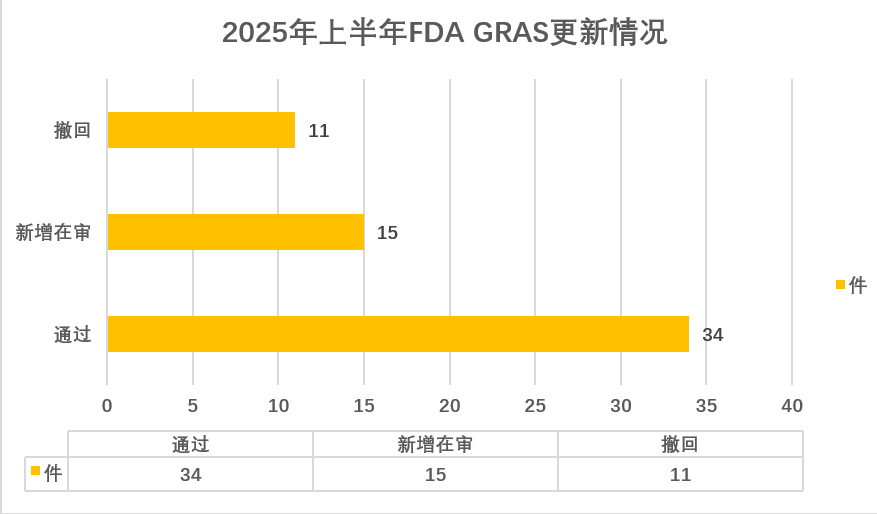
圖1 2025年上半年FDA GRAS申報情況
2.2025年上半年更新認證通過的物質(以FDA官網更新時間計):共34款
2025年第一、第二季度,更新“FDA has no questions”狀態的物質有34款。其中,微生物相關物質13款,其他類物質12款,代糖類原料5款,乳制品3款,HMO物質1款。申請公司來自美國、中國、韓國、日本、加拿大、荷蘭、愛爾蘭、印度、愛沙尼亞、智利等多個國家,其中美國和中國公司最為活躍。
需要說明的是,其中很多物質實際上很早就已經獲得了“FDA has no questions”,通過時間跨度大(2024.02.05~2025.03.14),大量卷宗于2024年下半年(6月至12月)獲批,少數獲批時間為2025年第一季度。但因為FDA官網更新的延遲,才剛剛被更新至官網中公開。
表1 2025年第二季度FDA官網更新FDA has no questions狀態的物質
序號 | GRN NO. | 中文名稱 | 類別 | 公司 | 通過時間 |
1 | 1069 | 玉米蛋白 | 其他 | Cargill, Inc.(美國) | 2024.02.05 |
2 | 1109 | 來自天藍色鏈霉菌的β-瓊脂糖酶制劑 | 微生物相關 | Dyne Bio Inc.(韓國) | 2024.04.15 |
3 | 1117 | 來自粗壯脈紋孢菌的菌絲生物質 | 微生物相關 | The Better Meat Co.(美國) | 2024.07.09 |
4 | 1120 | 黑曲霉生產的α-半乳糖苷酶制劑 | 微生物相關 | Novozymes North America(美國) | 2024.06.05 |
5 | 1122 | 濃縮油菜籽 | 其他 | NapiFeryn BioTech Sp. z o. o.(波蘭) | 2024.07.25 |
6 | 1126 | 乙酸鈣 | 其他 | Niacet Corporation(美國) | 2024.06.07 |
7 | 1129 | 熱滅活酪丁酸梭菌ASM#19 | 微生物相關 | Superbrewed Food, Inc.(美國) | 2024.02.22 |
8 | 1133 | 玉米抗性糊精 | 其他 | Anderson Global Group(美國) | 2024.01.22 |
9 | 1139 | 由攜帶來自茂原鏈霉菌的谷氨酰轉氨酶編碼基因的地衣芽孢桿菌生產的谷氨酰轉氨酶制劑 | 微生物相關 | Novozymes North America(美國) | 2024.07.02 |
10 | 1147 | 銅 (II)離子 | 其他 | Copperprotek SPA(智利) | 2024.07.05 |
11 | 1148 | D-阿洛酮糖 | 代糖類原料 | Daesang Corporation(韓國) | 2024.09.30 |
12 | 1151 | 蠶豆蛋白 | 其他 | Cooperative Koninklijke Cosun U.A.(荷蘭) | 2024.06.12 |
13 | 1154 | 由攜帶來自尖孢鐮刀菌的表達脂肪酶編碼基因巴斯德畢赤酵母生產的三酰甘油脂肪酶制劑 | 微生物相關 | Lallemand Inc.(加拿大) | 2024.08.15 |
14 | 1157 | 2'-巖藻糖基乳糖 | HMO | 虹摹生物科技(上海)有限公司(中國) | 2024.08.07 |
15 | 1159 | 凝結芽孢桿菌MTCC 25460孢子制劑 | 微生物相關 | Pellucid Lifesciences Pvt., Limited(印度) | 2024.05.06 |
16 | 1161 | 柱狀假絲酵母生產的三酰甘油脂肪酶制劑 | 微生物相關 | Meito Sangyo Co., Ltd.(日本) | 2024.09.24 |
17 | 1164 | 針對單核細胞增多性李斯特菌的化學合成的pediocin PA-1(廣譜乳酸菌細菌素)類似物 | 其他 | Innodal and Quality Systems Solutions(加拿大) | 2024.08.07 |
18 | 1166 | 蠶豆(Vicia faba L.)蛋白水解物 | 其他 | Nuritas(愛爾蘭) | 2024.11.13 |
19 | 1167 | 由表達來自Pentadiplandra brazzeana的巴西甜蛋白編碼基因的畢赤酵母生產的巴西甜蛋白制劑 | 代糖類原料 | Perfect Day, Inc.(美國) | 2024.10.08 |
20 | 1170 | 粉狀或糖漿狀木薯抗性糊精 | 其他 | Icon Foods, Inc.(美國) | 2024.10.22 |
21 | 1171 | 非動物 21 型膠原蛋白多肽 | 其他 | Geltor, Inc.(美國) | 2024.10.22 |
22 | 1174 | 干全脂羊奶 | 乳制品 | The LittleOak Company(美國) | 2024.12.06 |
23 | 1175 | 植物乳桿菌 DSM 23881 | 微生物相關 | Nordwise BioCC OÜ(愛沙尼亞) | 2024.10.22 |
24 | 1183 | 表達改良單胞菌素編碼基因的畢赤酵母 P-MON-040 產生的單胞菌素制劑 | 微生物相關 | Oobli, Inc.(美國) | 2024.11.22 |
25 | 1184 | 來自改造菌株大腸桿菌 BL21(DE3) 的瑞鮑迪苷M | 代糖類原料 | 四川盈嘉合生科技有限公司(中國) | 2024.10.23 |
26 | 1187 | 由表達來自白麴的內聚半乳糖醛酸酶編碼基因的里氏木霉生產的內聚半乳糖醛酸酶制劑 | 微生物相關 | AB Enzymes Inc.(美國) | 2025.02.28 |
27 | 1188 | D-阿洛酮糖 | 代糖類原料 | 山東星光首創生物科技有限公司(中國) | 2024.11.19 |
28 | 1190 | 表達來源于短芽孢桿菌的乙酰乳酸脫羧酶基因的釀酒酵母菌株 OYR-481 | 微生物相關 | Omega Yeast Labs, LLC(美國) | 2024.09.27 |
29 | 1191 | 表達來自粟酒裂殖酵母的麥角硫因合成酶的大腸桿菌 BL-21 (DE3)生成的麥角硫因 | 其他 | 上海麥角硫因生物科技集團有限公司(中國) | 2025.01.30 |
30 | 1197 | 由表達來自卷曲乳桿菌的果聚糖酶編碼基因的里氏木霉 AR-577 生產的果聚糖酶制劑 | 微生物相關 | AB Enzymes Inc.(美國) | 2025.03.14 |
31 | 1198 | 肌醇 | 其他 | 四川博浩達生物科技有限公司(中國) | 2025.02.03 |
32 | 1206 | 通過酶轉化處理從甜葉菊中提取得到的純化瑞鮑迪苷A生成瑞鮑迪苷M | 代糖類原料 | 弈柯萊生物科技(上海)股份有限公司(中國) | 2025.02.28 |
33 | 1211 | 低礦物質山羊乳清 | 乳制品 | Crossway Foods Limited(愛爾蘭) | 2025.02.04 |
34 | 1212 | 液態全脂山羊奶 | 乳制品 | Crossway Foods Limited(愛爾蘭) | 2025.02.07 |
注:GRN1187為GRN1110的重新提交,GRN1197為GRN1121的重新提交。
3. 2025年上半年申請撤回的物質及原因
截至2025年6月10日,2025年上半年共有10例撤回案例的更新,因FDA官網更新存在滯后性,這些卷宗多數在2024年進行撤回,但于2025年才在FDA網站上更新了撤回狀態,撤回情況如表1所示。
表1 2025年上半年FDA官網更新的卷宗撤回情況
GRN NO. | 中文名稱 | 類別 | 公司 | 時間 | 撤回主要原因 |
1141 | L-α-甘磷酸膽堿 | 其他 | Shenyang Gold Jyouki Technology Co., Ltd(中國) | 2024.04.29 | EDI數據和安全性數據不足。 |
1152 | 肺形側耳菌絲體生物質 | 其他 | Mushlabs GmbH(德國) | 2024.03.21 | 實體和菌絲體之間之間潛在基因表達差異的數據和信息所導致不同的食用安全性的問題 |
1153 | 水黃皮豆油 | 其他 | Terviva, Inc.(美國) | 2024.05.23 | 物質體現出了藥物功能。 |
1160 | 浮萍葉蛋白 | 其他 | Plantible Foods (美國) | 2024.05.06 | 關鍵安全性數據非公開。 |
1163 | 一種含有兩種腸炎沙門氏菌特異性噬菌體(噬菌體)的制劑 | 微生物相關 | Cytophage Technologies inc.(加拿大) | 2024.05.28 | 生產工藝變更。 |
1168 | 虎耳草粉 | 其他 | Tigernut Traders, SL(西班牙) | 2024.08.06 | 安全性數據存疑,動物實驗折算倍數,動物安全性試驗只有雌鼠。 |
1169 | 6'-唾液乳糖鈉鹽 | HMO | GeneChem, Inc.(韓國) | 2024.10.07 | 產品中可能有鋰,缺乏在生產過程中去除雜質的詳細信息、為支持成分成分分析而提供的數字難以辨認,以及有關預期用途和由此產生的膳食暴露估計值的問題。 |
1176 | 乳糖-N-四糖 | HMO | FrieslandCampina Ingredients B.V.(荷蘭) | 2024.09.24 | LNT 的成分、缺乏有關最終產品中雜質的數據和信息,以及發酵培養基中使用鈷引起的其他問題。 |
1180 | 纖維二糖 | 代糖類原料 | SAVANNA Ingredients GmbH(德國) | 2024.09.09 | 生產工藝的細節缺失,有關預期用途和膳食暴露估計值的問題,以及纖維二糖在幼兒中的耐受性和安全性的數據和信息的不足。 |
1194 | 提取自雞蛋的部分水解蛋骨素 | 其他 | ESM Technologies, LLC(美國) | 2025.02.04 | 現有安全性數據不足,關鍵信息缺失(蛋白質特性、過敏原信息、精確暴露量計算、長期影響評估),還需明確使用范圍,關注砷含量。 |
4.2025年上半年中國企業提交物質情況
在本次更新中,中國企業共有9款物質狀態進行了更新。其中,6款獲得“FDA has no questions”回復,2款物質為新增在審,1款物質為撤回。涉及的物質包括HMO、代糖類物質、微生物相關物質和其他營養補充劑。
表2 2025年上半年FDA 官網更新的中國企業提交物質情況
序號 | GRN NO. | 中文名稱 | 類別 | 公司 | 狀態 | 更新時間 |
1 | 1141 | L-α-甘磷酸膽堿 | 其他 | 沈陽金久奇科技有限公司 | 撤回 | 2024.04.29 |
2 | 1157 | 2'-巖藻糖基乳糖 | HMO | 虹摹生物科技(上海)有限公司 | 通過 | 2024.08.07 |
3 | 1184 | 來自改造菌株大腸桿菌 BL21(DE3) 的瑞鮑迪苷M | 代糖類原料 | 四川盈嘉合生科技有限公司 | 通過 | 2024.10.23 |
4 | 1188 | D-阿洛酮糖 | 代糖類原料 | 山東星光首創生物科技有限公司 | 通過 | 2024.11.19 |
5 | 1191 | 表達來自粟酒裂殖酵母的麥角硫因合成酶的大腸桿菌 BL-21 (DE3)生成的麥角硫因 | 其他 | 上海麥角硫因生物科技集團有限公司 | 通過 | 2025.01.30 |
6 | 1198 | 肌醇 | 其他 | 四川博浩達生物科技有限公司 | 通過 | 2025.02.03 |
7 | 1206 | 通過酶轉化處理從甜葉菊中提取得到的純化瑞鮑迪苷A生成瑞鮑迪苷M | 代糖類原料 | 弈柯萊生物科技(上海)股份有限公司 | 通過 | 2025.02.28 |
8 | 1230 | 香蘭素 | 其他 | 四川盈嘉合生科技有限公司 | 在審 | / |
9 | 1232 | 副干酪乳桿菌DSMZ 28047 | 微生物相關 | 晨暉生物科技股份有限公司 | 在審 | / |
5.總結
FDA在2025年上半年的更新中集中更新了2024年的申報情況,獲批物質量大幅上升,中國企業依然積極申報,維持了在代糖類物質申報中的強勢表現,在HMO、微生物和功能性原料等領域多點開花。為提高物質獲批率,瑞旭集團建議,企業在準備GRAS卷宗時,提供充分的安全性評價數據,設立可靠的物質指標,計算合理的膳食暴露量以確保物質安全性。瑞旭集團也將為企業提供全面服務助力GRAS申報。
*數據來源:FDA官網GRAS清單及最新發布受理的GRAS卷宗(更新時間2025/06/10)。
*注:1. 由于FDA不披露關于卷宗受理時間,因此在審物質統計的數據主要以發布卷宗中的提交申報時間為準。
2.本文數據以官方受理并公開發布可查詢GRAS編號的卷宗統計,數據僅供參考。
