2017年首次進口非特殊化妝品合規流程
1.產品從上海浦東新區口岸進口,且境內責任人注冊地在浦東新區
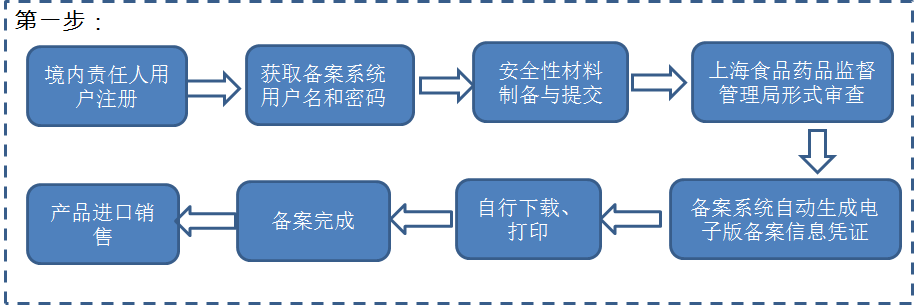
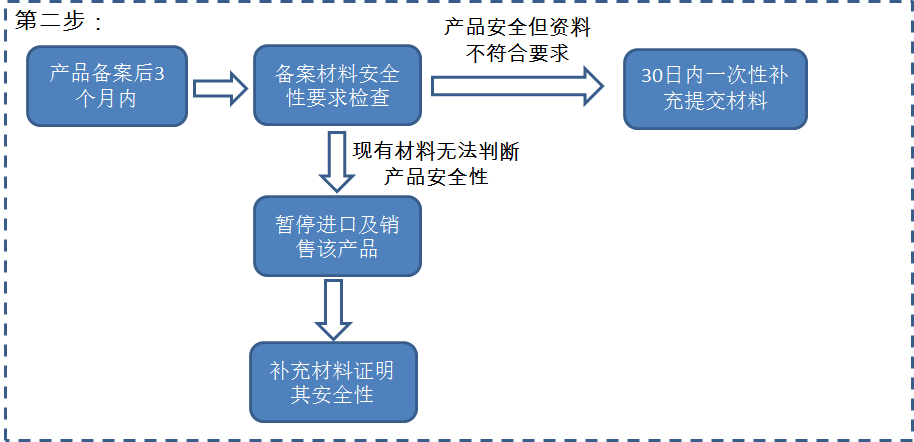
2.產品從上海浦東新區以外口岸進口
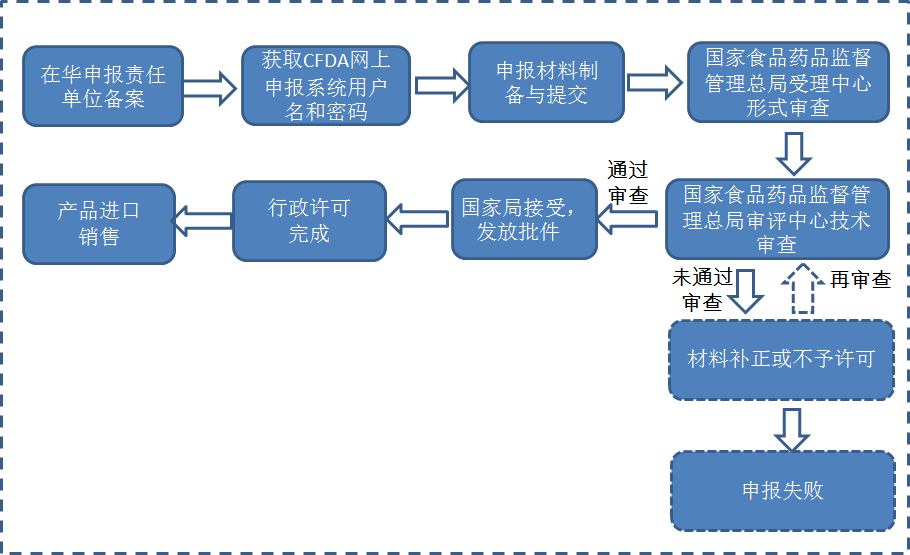
3.不再從上海浦東新區口岸進口的已備案產品
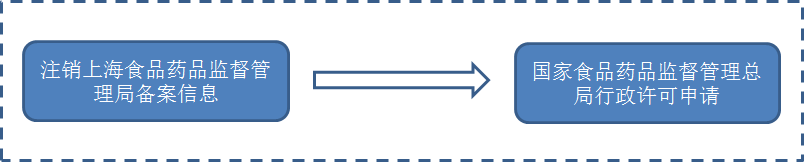
4.產品從上海浦東新區等多個口岸進口
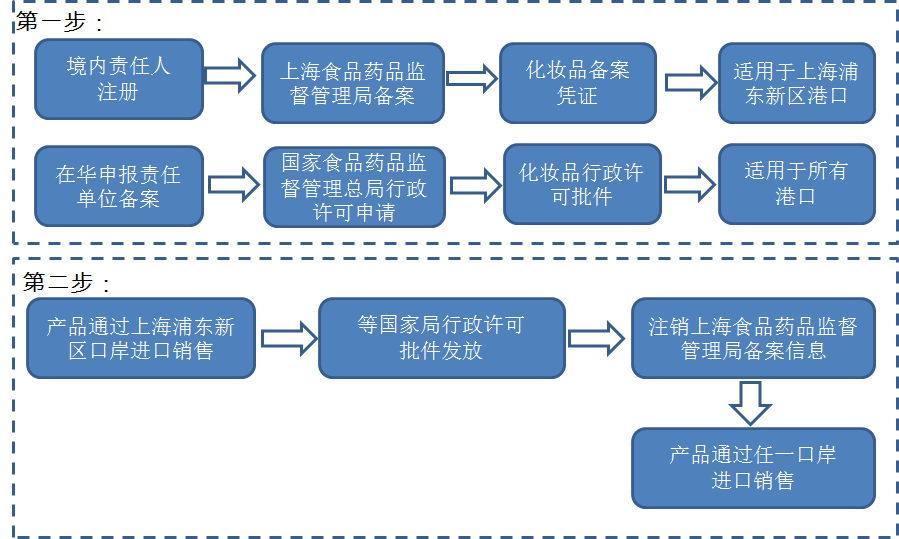
由此看出,2017年企業可以根據實際情況對首次進口非特殊用途化妝品采用不同方式進行市前備案或許可。而特殊用途化妝品仍需要在國家局進行行政審批。以下表格匯總了針對產品類型、進口口岸及企業特點可供企業選擇的備案或許可方式。
| 產品類型 | 進口口岸 | 是否在浦東新區注冊公司 | 銷售模式 | 市前準入方案 |
| 進口非特殊 | 上海浦東新區 | 有 | 線下 | 上海食品藥品監督管理局進行備案申請 |
| 進口非特殊 | 上海浦東新區或者多個口岸 | 無 | 線下 | 國家局行政許可申請 |
| 進口非特殊 | 上海浦東新區等多口岸 | 有 | 線下 | 上海食品藥品監督管理局備案申請與國家局行政許可申請可同時開展。上海局備案完成后產品可先從浦東新區口岸進口銷售。等國家局行政許可申請下來,可注銷上海局備案信息,產品仍可在浦東新區及其他任一口岸進口銷售 |
| 進口特殊 | - | - | 線下 | 國家局行政許可申請 |
| 國產特殊 | - | - | 線下 | 國家局行政許可申請 |
| 國產非特 | - | - | 線下 | 地方局備案申請 |
| 進口化妝品 | - | - | 線上 | 天津、上海、杭州、寧波、鄭州、廣州、深圳、重慶、福州、平潭等10個試點城市至2017年12月31日前無需行政許可 |
| 項目 | 國家局行政許可 | 上海局備案 |
| 主管部門 | 國家食品藥品監督管理總局 | 上海食品藥品監督管理局 |
| 授權申請 | 國外申請人授權在華公司作為在華申報責任單位 | 國外申請人授權在華公司作為境內責任人 |
| 在華公司要求 | 注冊地無限制 | 浦東新區注冊 |
| 在華公司責任 | 僅負責產品行政許可 | 負責產品進口和經營,并承擔產品質量安全責任 |
| 適用范圍 | 全國各口岸 | 上海浦東新區 |
| 用戶名密碼申請 | 國家局行政許可系統 | 上海局備案系統 |
| 用戶名密碼申請資料 | -申請表 -授權書公證與翻譯件 -在華申報責任單位營業執照 | -申請書 -授權書公證與翻譯件 -境內責任人營業執照 |
| 行政許可或備案材料 | (一)申請表; (二)產品中文名稱命名依據; (三)產品配方; (四)產品質量安全控制要求; (五)產品原包裝; (六)經衛生部認定的檢驗機構出具的檢驗報告及相關資料; (七)產品中可能存在安全性風險物質的有關安全性評估資料; (八)已經備案的行政許可在華申報責任單位授權書復印件及營業執照復印件并加該公章; (九)化妝品使用原料及原料來源符合瘋牛病區高風險物質禁限用要求的承諾書; (十)自由銷售證明; (十一)可能有助于評審的其它資料; (十二)生產工藝簡述和簡圖; (十三)化妝品產品技術要求的文字版資料。 提供原件1份,另附未啟封的市售樣品1件。 | (一)申請表; (二)產品中文名稱命名依據; (三)產品配方; (四)產品質量安全控制要求; (五)產品原包裝圖片; (六)產品生產工藝簡述; (七)產品技術要求; (八)化妝品行政許可檢驗機構出具的檢驗報告及相關資料; (九)產品中可能存在安全性風險物質的有關安全性評估資料; (十)化妝品適用原料及原料來源符合瘋牛病疫區高風險物質禁限用要求的承諾書; (十一)自由銷售證明; (十二)境外生產企業生產質量管理的相關證明材料; (十三)參照《化妝品行政許可申報受理規定》(國食藥監許〔2009〕856號,以下稱《申報受理規定》)要求,可能有助于備案的其他資料 |
| 資料形式審查機構 | 國家局行政受理中心 | 上海食品藥品監督管理局 |
| 技術審查 | 形式審查后移交總局保健食品審評中心進行技術審查 | 產品備案后3個月內開展 |
| 許可或者備案憑證 生成流程及形式 | 技術審查通過后發放行政許可批件證書 | 形式審查通過后備案系統自動生成電子版備案信息憑證供企業自行下載打印 |
| 批準或備案憑證編號格式 | 國妝備進字J+四位年份數字+四位編號 | 國妝網備進字(滬)+四位年份數字+六位順序編號 |
| 批準或備案憑證 有效期 | 4年 | 未知 |
| 已批準或備案產品 不再進口 | 無要求 | 境內責任人注銷備案信息 |
由上表看出,國家局行政許可與上海局備案模式最大的差異體現在許可或備案流程及境內責任人的要求。上海局備案最大優勢體現在企業通過資料形式審查后就可以獲得備案號進行進口銷售。國家局行政許可要求在通過所有形式和技術審查后才能獲得許可號進行進口銷售。兩者相比,前者更利于企業將產品快速投放市場。更多加強市后監管。但在資料要求上,兩者幾乎保持一致。雖然新的備案工作程序要求已經發布,但在實際操作中無論企業還是主管部門仍然將面臨很多未知的問題。至少從法規層面看出政府希望保持相同技術審評尺度,只是調整許可程序和監管方式。除此之外,新的備案方式對境內責任人的要求較高。需要境內責任人承擔產品的進口和經營,并同時承擔產品的質量安全責任。而傳統許可方式的在華申報責任單位僅限于對產品申報相關事項承擔責任。由此看出,境內企業在選擇新的備案方式前需謹慎考慮產品上市后的質量安全風險。總之,由上海浦東新區試點實施首次進口非特殊用途化妝品備案模式看出,政府已經對2016年第24號文件及2015年食品藥品監管總局關于對取消和下放行政審批事項加強事中事后監管的意見作出響應和落實。
