一、韓國醫療器械注冊
l 韓國醫療器械監管機構
MFDS:Ministry of Food and Drug Safety 韓國食品藥品安全部
l 韓國醫療器械證書持有人
非韓國境內的醫療器械制造商,必須指定一家韓國境內注冊企業作為其韓國許可證持有人(Korea License Holder, KLH)。由 KLH 向 MFDS 申請其醫療器械的注冊和 KGMP 認證等程序。
l 韓國醫療器械分類
區分 | 備案 | 認證 | 許可 |
I類 | O | - | O *與已備案醫療器械在結構等方面不具有實質性等同的醫療器械 |
II類 | - | O | O *與已認證醫療器械在結構等方面不具有實質性等同的醫療器械 *MFDS指定的需要許可的醫療器械 |
III類 | - | - | O |
IV類 | - | - | O |
l 韓國醫療器械證書有效期
5年(包括備案、認證、許可證書),有效期屆滿180天前提交延續申請。
l 韓國醫療器械注冊流程(首次)

*NIDS:National Institute of Medical Device Safety Information
*MFDS:Ministry of Food and Drug Safety
*MFDS指定的第三方審查機構(8個):NIDS,KTL,KTC,KTR,KCL,韓國SGS, Kmedihub, YONSEI UNIVERSITY HEALTH SYSTEM Dental Device Testing and Evaluation Center.
l 費用
MFDS注冊官費
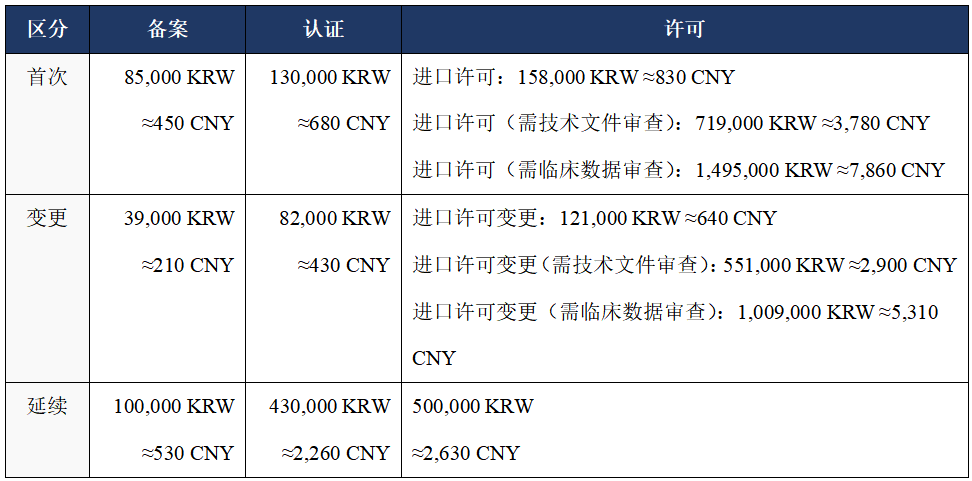
*上述費用適用于,醫療器械進口備案/認證/許可
醫療器械技術文件審查費
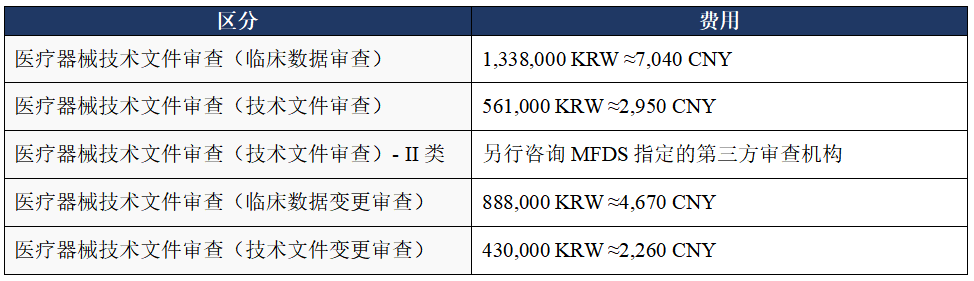
l 語言
韓語、英語
l 韓國MFDS證書格式

二、 KGMP
l KGMP適用對象
醫療器械制造商&進口商
- I類醫療器械:非必須/非強制
- II,III,IV類醫療器械:必須/強制
l KGMP證書有效期
KGMP 證書有效期為3年,證有效期屆滿3個月前提交延續申請(即定期審查)。
l KGMP審查流程
* 表示“如需”
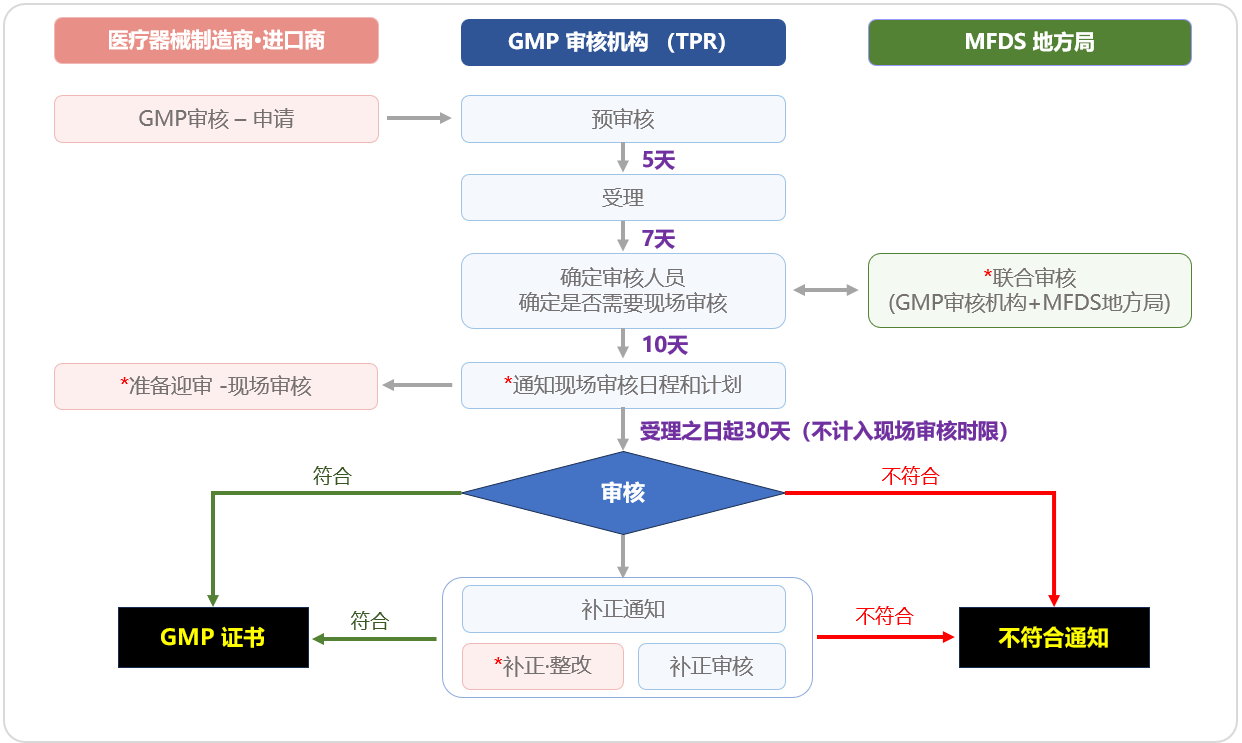
l KGMP審查方式及審核機構
區分 | 首次審核 | 附加審核 | 變更審核 | 定期審核(延續) | |
II類 | 審核機構 | 獨立審核 (TRP) | 獨立審核 (TRP) | 獨立審核 (TRP) | 獨立審核 (TRP) |
審核方式 | 資料 + 現場 | 資料 | 資料 + 現場 | 資料 + 現場 | |
III類 | 審核機構 | 獨立審核 (TRP) | 獨立審核 (TRP) | 獨立審核 (TRP) | 獨立審核 (TRP) |
審核方式 | 資料 + 現場 | 資料 | 資料 + 現場 | 資料 + 現場 | |
IV類 | 審核機構 | 聯合審核 (TPR + MFDS地方局) | 聯合審核 (TPR + MFDS地方局) | 聯合審核 (TPR + MFDS地方局) | 聯合審核 (TPR + MFDS地方局) |
審核方式 | 資料 + 現場 | 資料 | 資料 + 現場 | 資料 + 現場 | |
* TRP:Third Party Review / 第三方審核
l KGMP審核機構
序號 | KGMP審核機構 (Third Party Review / 第三方審核) | |
1 | ?????????(?) | TUV SUD Korea Ltd. |
2 | ???????????(?) | TUV Rheinland Korea Ltd. |
3 | ????????? | Korea Testing Laboratory |
4 | ??????????? | Korea Testing & Research Institute |
5 | ????????????? | Korea Testing Certification |
6 | (?)????????????? | Korea Conformity Laboratories |
l KGMP證書格式

三、我們的服務
1. 醫療器械MFDS注冊與認證
產品評估與分類咨詢:準確判定產品的分類,并規劃最有效的符合性評價路徑。
數據缺口分析:系統評估現有技術文件、質量管理體系與認證要求的差距,提供清晰的改進路線圖。
系統化技術文件構建:系統化地整理和編寫認證必須資料,包括產品說明書、標簽、設計驗證報告、風險分析報告(符合ISO 14971)、滅菌驗證、軟件驗證(如適用)等。
充當溝通橋梁:負責與CAB機構進行高效、專業的溝通,包括前期接洽、資料提交、問詢回復及審核安排,確保流程順暢。
2. 醫療器械KGMP建立與優化
體系建立與整合: 協助建立全新的、符合要求的QMS。
體系升級與優化: 將MFDS的要求(如上市后監督、供應商控制、UDI等)無縫整合到現有QMS中。
模擬審核與培訓: 提供公告機構審核前的模擬審核,并針對關鍵崗位人員進行法規和質量管理培訓,提升團隊整體合規能力。
3. 韓國許可證持有人(KLH)
韓國許可證持有人(KLH):提供具有符合要求且具有合規能力的許可證持有人服務。
