一、什么是玻尿酸?
玻尿酸是透明質酸鈉的俗稱,又名玻璃酸鈉,是由N-乙酰葡萄糖醛酸反復交替而形成的一種高分子多糖體生物材料。在醫學整形中作為注射用軟組織填充劑,用于注射到皮膚真皮層或皮下組織內,達到糾正皺紋,改善皮膚外觀的作用。
二、玻尿酸的管理類別如何(是藥品還是醫療器械)?
- 用于治療關節炎、干眼癥、皮膚潰瘍等具有確定的藥理作用的產品,按照藥品管理;
- 用于輔助眼科手術產品、外科手術防粘連產品、填充增加組織容積(美容填充)等的產品,按照醫療器械管理。
三、玻尿酸市場監管情況如何?
作為醫療器械管理的注射用透明質酸鈉如今被廣泛用于除皺、豐唇、隆鼻等非手術微整形中,但是目前市場中的不法分子非法制售和使用注射用透明質酸鈉謀取利益,對消費者造成了極大的危害。為保障用械安全,CFDA一直堅持整頓市場并取得了顯著的成效。2015年10月14日,CFDA再次啟動整頓計劃(開展打擊非法制售和使用注射用透明質酸鈉行為專項行動工作方案)。
本次整頓計劃由CFDA牽頭,聯合工業和信息化部、公安部、國家衛生計生委和國家工商總局等部門,重點查處一批大案要案,曝光一批非法制售和使用注射用透明質酸鈉的企業和單位,對相關企業整頓的內容和措施如下:
| 序號 | 部門 | 監査對象 | 重點檢查的違法類型 | 違法處罰 | |||||||||||||||
| 1 | CFDA及各級藥監局 | 注射用透明質酸鈉生產企業、經營企業和使用單位 | 無證行為: 1. 未取得醫療器械注冊證組織生產的; 2. 未取得醫療器械生產許可證組織生產的; 3. 未取醫療器械經營許可證從事經營的; 4. 經營無證(注冊證或生產許可證)產品的; 5. 使用無證(注冊證或生產許可證或經營許可證)產品; 6. 證書有效期已屆滿未進行延續申請的; 7. 使用無合格證明文件、過期、失效、淘汰的醫療器械,或者使用未依法注冊的醫療器械的等。 | ①沒收違法所得、違法生產/經營的醫療器械和用于違法生產/經營的工具、設備、原材料等; ②罰款: 若貨值不足1萬元,處5萬~10萬元罰款; 若貨值金額1萬元以上,處貨值金額10~20倍罰款; ③情節嚴重的,5年內不受理相關責任人及企業提出的醫療器械許可申請; ④對于生產/經營無醫療器械注冊證的行為,若情節嚴重,吊銷原生產許可證/經營許可證。 | |||||||||||||||
| 2 | 衛生計生部門 | 美容醫療機構 | 未取得《醫療機構執業許可證》開展醫療美容服務的行為。 | ①責令其停止執業活動; ②沒收非法所得和藥品、器械,并處以三千元以下的罰款;情節嚴重的處以三千元以上。一萬元以下的罰款。 | |||||||||||||||
| 3 | 工商行政管理部門 | 美容院 | 1. 涉嫌未取得《醫療機構執業許可證》開展醫療美容的,依法移送衛生計生部門; 2. 涉嫌未取得《醫療器械經營許可證》經營注射用透明質酸鈉的,依法移送藥監局 | ①若查實未取得《醫療機構執業許可證》,參照 “2”中的罰則; ②若查實未取得《醫療器械經營許可證》從事經營活動,參照“1”中的罰則 | |||||||||||||||
| 4 | 通信主管部門 | 互聯網 | 1. 利用互聯網發布虛假違法信息 2. 擅自從事醫療器械互聯網信息和交易服務且拒不整改的 | ①責令停止發布廣告,責令廣告主在相應范圍內消除影響; ②罰款:
| |||||||||||||||
| 5 | 公安機關 | 立案偵查非法制售和使用注射用透明質酸鈉涉嫌犯罪的案件 | 依據相應違法類型立案偵查 | ||||||||||||||||
四、玻尿酸產品市場準入和使用等環節需要哪些證件?
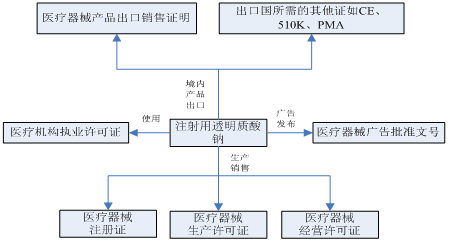
在注射用透明質酸鈉生產、宣傳、銷售、使用、出口等活動中,相關企業應該依據相關法規的規定取得相應的證件,下圖列舉了玻尿酸在不同生命階段所需取得的相應證件:
| 證件 | 批準部門 | 有效期 |
| 醫療器械注冊證 | CFDA | 5年 |
| 醫療器械生產許可證 | 所在地省級FDA | 5年 |
| 醫療器械經營許可證 | 所在地市級FDA | 5年 |
| 醫療器械廣告批準文號 | 所在地省級FDA | 1年 |
| 醫療機構執業許可證 | 所在地縣級以上衛計委 | 定期校驗 |
| 醫療器械出口銷售證明 | 所在地省級FDA | 不應超過申報資料提交的各類證件最先到達的截止日期,且最長不超過2年。 |
| 備注:生產企業預計在所在轄區銷售自己的產品,無需取得經營許可證, | ||
綜上所述,預計從事注射用透明質酸鈉或其他醫療器械的生產、銷售、使用、出口等活動時,應嚴格恪守法規規定,取得合法資質證件,相關玻尿酸注冊和經營問題,歡迎咨詢瑞旭技術專家。
