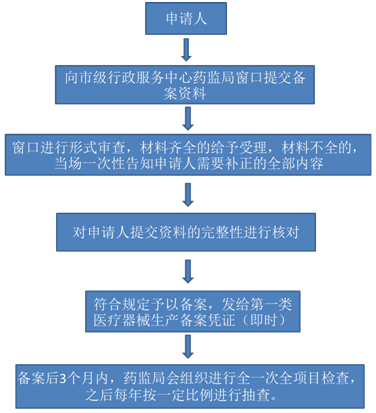
- 一類醫療器械生產企業相關備案流程
- 第一類醫療器械生產企業備案相關法規:
- 2013年11月26日,國家食品藥品監管總局關于印發體外診斷試劑分類子目錄的通知(食藥監械管〔2013〕242號);
- 2014年5月30日,關于發布第一類醫療器械產品目錄的通告(國家食品藥品監督管理總局令第8號);
- 2014年5元30日,國家食品藥品監督管理總局關于醫療器械生產經營備案有關事宜的公告(第25號)
- 2014年7月30日,《醫療器械生產監督管理辦法》(國家食品藥品監督管理總局令第7號);
- 2014年7月30日,《醫療器械說明書和標簽管理規定》(國家食品藥品監督管理總局令第6號);
- 2014年9月26日,食品藥品監管總局辦公廳關于啟用醫療器械生產經營許可備案信息系統的通知
- 2014年9月30日,食品藥品監管總局關于印發醫療器械生產企業分類分級監督管理規定的通知
- 2015年6月29日,《藥品醫療器械飛行檢查辦法》(國家食品藥品監督管理總局令第14號)
- 第一類醫療器械生產企業申請條件
- 企業已取得第一類醫療器械產品備案憑證;
- 企業已取得工商《營業執照》在有效期內;
- 具備與所生產產品相應的生產場地、環境條件、基礎設施;
- 具備與所生產產品相應的技術人員、檢驗儀器、管理制度、售后服務能力;
- 一類醫療器械生產企業備案提交相關資料
- 第一類醫療器械生產備案表;
- 所生產產品的醫療器械備案憑證復印件;
- 營業執照和組織機構代碼證復印件;
- 法定代表人、企業負責人身份證明復印件;
- 生產、質量和技術負責人的身份、學歷、職稱證明復印件;
- 生產管理、質量檢驗崗位從業人員學歷、職稱一覽表;
- 生產場地的證明文件,有特殊生產環境要求的還應當提交設施、環境的證明文件復印件;
- 主要生產設備和檢驗設備目錄;
- 質量手冊和程序文件目錄;
- 工藝流程圖;
- 經辦人授權證明;
- 其他證明性材料
- 一類醫療器械生產備案憑證

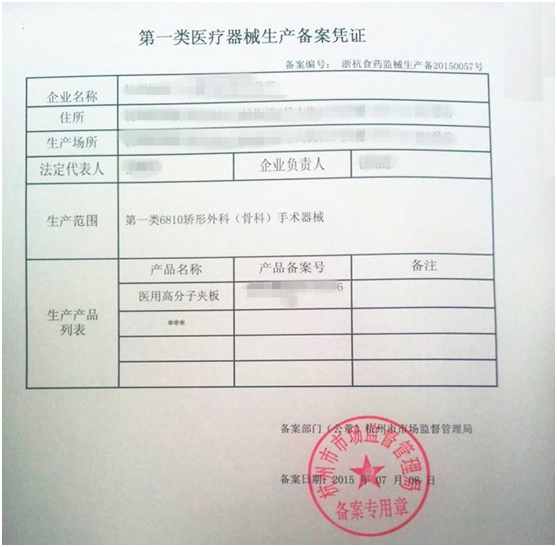
第一類醫療器械生產備案憑證的備案號編號規則為:XX食藥監械生產備XXXXXXXX號。其中:第一位X代表備案部門所在地省、自治區、直轄市的中文簡稱,第二位X代表所在地設區的市級行政區域的中文簡稱,第三到六位X代表4位數備案年份,第七到十位X代表4位數備案流水號。
- 一類醫療器械生產企業監督管理
第一類醫療器械生產企業在備案后3個月內,藥監局會組織進行全一次全項目檢查,之后每年按一定比例進行抽查。
若在現場檢查中,發現企業存在以下問題,則將對企業進行一定的處罰。
| 違法行為 | 處罰措施 |
| 利用虛假資料或其他欺騙手段取得醫療器械備案憑證 | ①向社會公告備案單位和產品名稱; ②情節嚴重的,直接責任人員5年內不得從事醫療器械生產經營活動 |
| 醫療器械生產備案憑證若偽造、變造、買賣、出租、出借 | ①責令改正; ②處1萬元以下罰款 |
| 生產無醫療器械備案憑證產品 | ①責令限期改正; ②逾期不改正的,向社會公告未備案單位和產品名稱,可以處1萬元以下罰款 |
| 生產不符合強制性標準或者備案的產品技術要求的產品; | ①責令改正,沒收違法生產的醫療器械; ②罰款: 貨值金額不足1萬元,處2萬~5萬元罰款; 貨值金額1萬元以上的,處貨值金額5~10倍罰款; ③情節嚴重的,責令停產停業,直至由原發證部門吊銷醫療器械備案憑證。 |
| 未按照備案的產品技術要求組織生產,或者未按規定建立質量管理體系并保持有效運行的 | |
| 違規委托生產,或未對受托方的生產行為進行管理 |
