一、 受理通知書、行政審批省局繳費通知書下載
第二類醫療器械首次注冊、第二類醫療器械變更注冊、第二類醫療器械延續注冊事項申請,在受理中心受理資料之后會相應生成《受理通知書》《行政審批繳費通知書》,各企業可通過接收到的受理或繳費短信通知內的網址登錄系統查看下載。使用chrome或360安全瀏覽器等瀏覽器急速模式,打開系統網址(http://qcwb.zjfda.gov.cn/)。
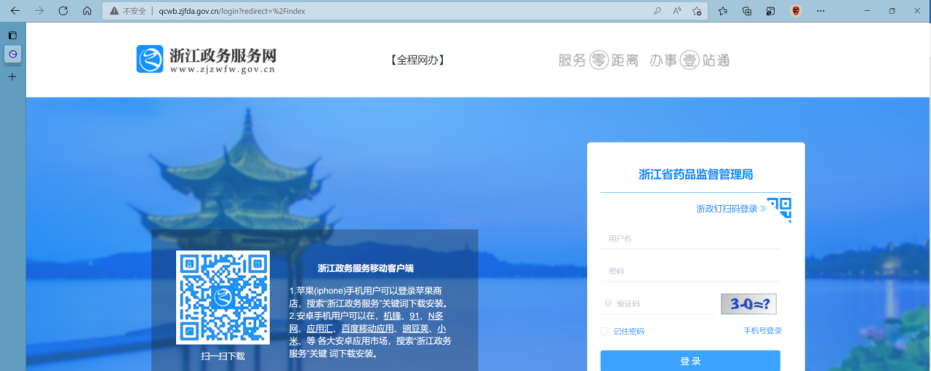
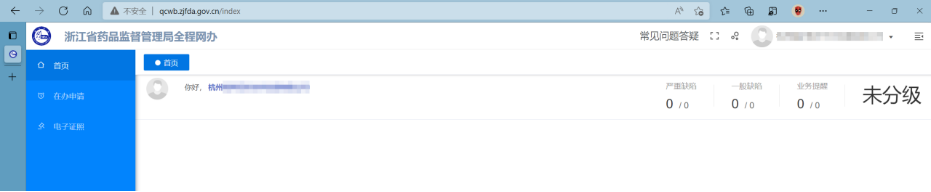
使用原浙江省藥品監督管理局行政審批系統的賬號密碼登錄,全程網辦系統不需要使用UKey識別賬號登錄,可直接輸入賬號以及密碼登錄系統。大多數企業賬號為SQ或JQ開頭的,如SQ33000001。若使用原密碼登錄提示密碼錯誤的,可將賬號作為密碼嘗試是否能登入系統,如賬號:SQ33000001,密碼:SQ33000001。如果還是登錄不了系統,可電話0571-88903259,或qq1611607245、3148183981聯系查詢賬號密碼。登入系統后界面如下。
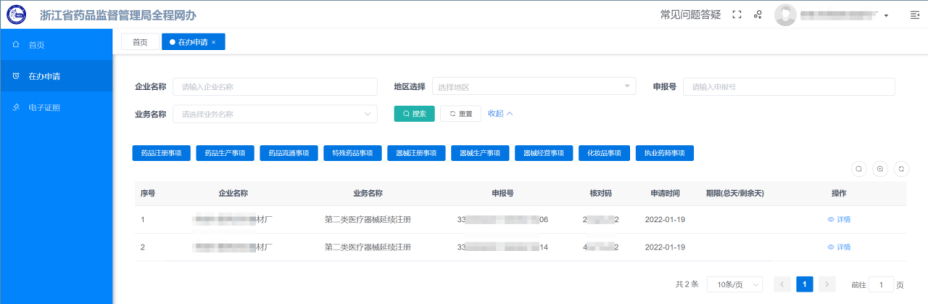
點擊左側菜單【在辦申請】進入查看當前申報的辦件,列表會展示當前正在辦理的所有企業申請,通過點擊詳情進入查看。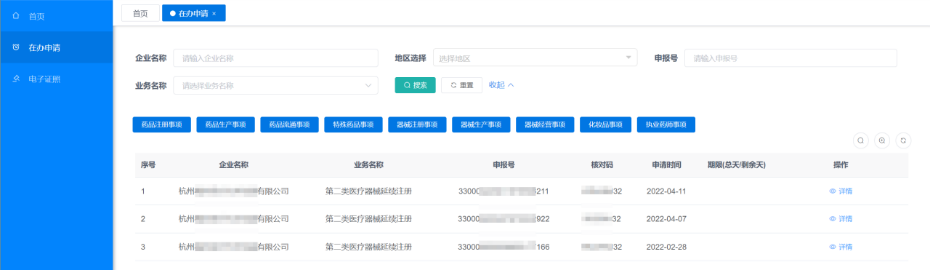
點擊“查看”按鈕進入辦件詳情頁,在此界面就可查看/下載相應的受理通知書或者繳費通知書。
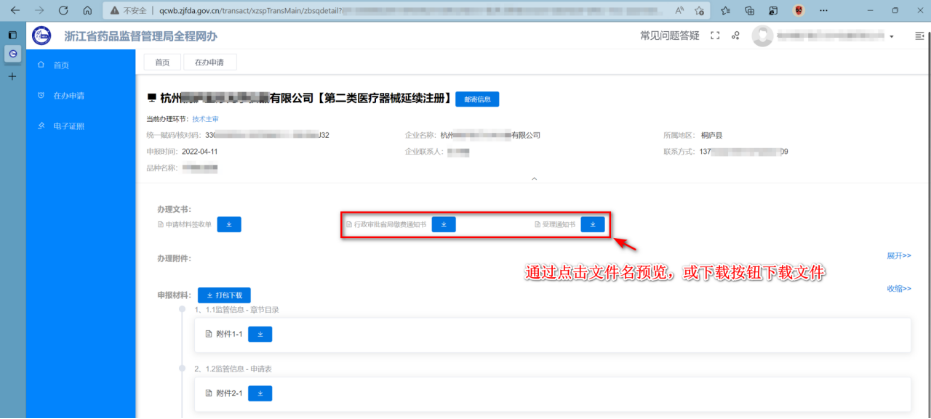
二、 技術審評一次性告知書下載,及資料補正
當主審對辦件進行技術審評發補后,企業需登錄系統提交相應的補正材料。如何登錄與第一點操作方式一致。登錄系統后同樣在【在辦申請】菜單進行操作。
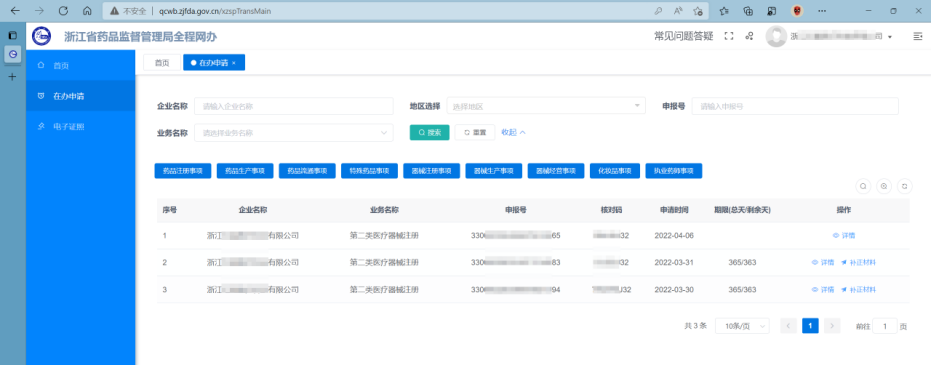
通過點擊“詳情”按鈕進入查看或下載《技術審評一次性告知書》。
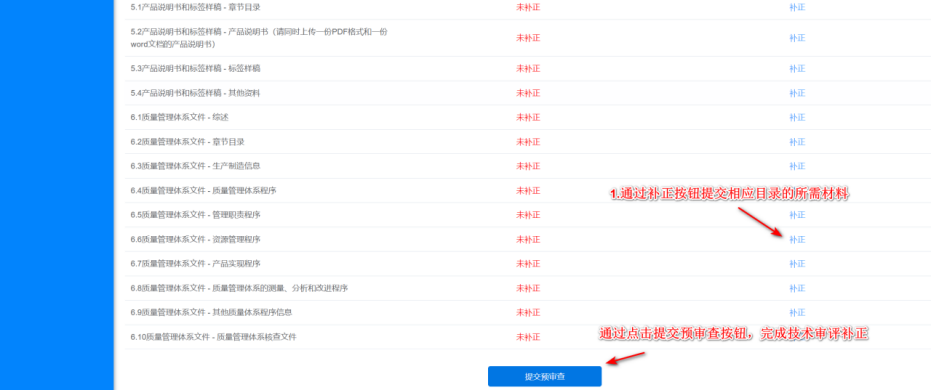
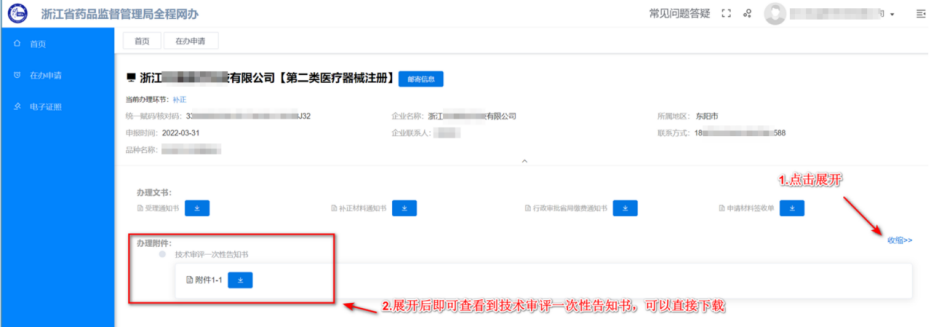 補正材料準備好之后,可登錄系統在【在辦申請】菜單,通過點擊“補正材料”按鈕進入材料提交頁,通過點擊各目錄右側“補正”按鈕提交相應文件材料,待材料全部上傳完成后,點擊頁面下方“提交預審查”按鈕將電子資料上報給主審。
補正材料準備好之后,可登錄系統在【在辦申請】菜單,通過點擊“補正材料”按鈕進入材料提交頁,通過點擊各目錄右側“補正”按鈕提交相應文件材料,待材料全部上傳完成后,點擊頁面下方“提交預審查”按鈕將電子資料上報給主審。
資料提交后辦件如圖所示,“補正材料”按鈕消息,證明資料已經提交。