紅外額溫計是用紅外方法測量患者額頭部位溫度來觀察患者體溫變化,通常由紅外溫度傳感器、探頭套、顯示單元、供電電路、測量電路組成,采用紅外感溫方法測量溫度顯示或者數據輸出。額溫計作為第二類醫療器械,生產、銷售應依據醫療器械法規首先完成注冊申報,瑞旭集團結合醫療器械法規及額溫計的注冊申報要求總結了額溫計產品的注冊申報過程的技術要求供參考。
依據醫療器械法規,額溫計屬于第二類醫療器械,分類編碼為07-03-04.3 體溫測量設備。
一、額溫計產品概述
1. 額溫計結構組成:
通常由紅外溫度傳感器、探頭套、顯示單元、供電電路、測量電路組成。
2. 額溫計工作原理:
自然界中一切溫度高于絕對零度(—273℃)的物體都會輻射出紅外線,而輻射出的紅外線的能量和溫度是正比的關系。利用這種關系,可以通過測量物體的紅外線強度來計算出它的溫度。采用紅外感溫方法測量溫度顯示或者數據輸出。
3. 額溫計典型結構:
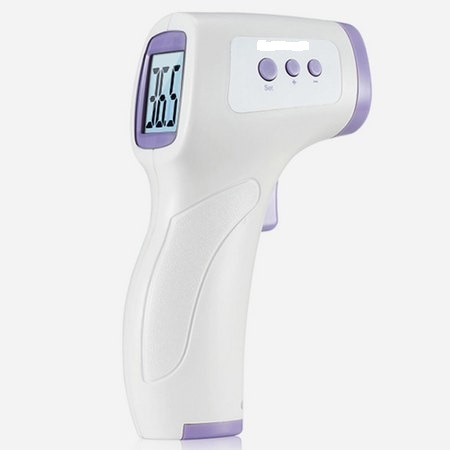
二、額溫計產品分類信息
一級 | 二級 | 三級 | 產品描述 | 預期用途 | 品名舉例 | 管理類別 |
07醫用診察和監護器械 | 03生理參數分析測量設備 | 04體溫測量設備 | 通常由紅外溫度傳感器、探頭套、顯示單元、供電電路、測量電路組成。采用紅外感溫方法測量溫度顯示或者數據輸出。 | 用紅外方法測量臨床測量患者體溫,通常用于測量患者耳道、額頭部位溫度。 | 電子體溫計、額溫計、紅外耳溫計 | Ⅱ |
三、額溫計臨床試驗要求
額溫計產品已經列入免于進行臨床試驗的醫療器械目錄中,可免于進行臨床試驗,但應提供臨床準確性的臨床驗證資料,免于進行臨床試驗的描述如下:
序號 | 分類編碼 | 產品名稱 | 產品描述 | 類別 |
353 | 07-03-04 | 額溫計 | 通常由紅外溫度傳感器、探頭套、顯示單元、供電電路、測量電路組成。采用紅外感溫方法測量溫度顯示或者數據輸出。應提供臨床準確性的臨床驗證資料。 | Ⅱ |
四、額溫計技術要求
1 外觀與結構
1.1 體溫計外形應端正,表面光亮整潔,不得有明顯的劃痕,破損和變形。
1.2 體溫計的控制面板上文字和標志應準確,清晰,牢固。
1.3 體溫計的控制和調節機構應靈活可靠,緊固件應無松動。
1.4 體溫計的功能鍵應有明確的標記,指示。
2. 溫度顯示范圍
體溫計溫度顯示范圍32.0℃~42.5℃。
3. 最大允許誤差
3.1 規定的溫度顯示范圍內最大允許誤差
體溫計在35.0℃~42.0℃的溫度顯示范圍內,最大允許誤差±0.2℃。
3.2 規定的溫度顯示范圍外最大允許誤差
體溫計在35.0℃~42.0℃的溫度顯示范圍外,最大允許誤差±0.3℃。
3.3 變化環境條件下最大允許誤差
變化環境下,體溫計在35.0℃~42.0℃的溫度顯示范圍內最大允許誤差應符合2.3.1的要求。
4. 抗跌落性
體溫計在正常使用時從垂直距離為1m高處以三次不同起始狀態自由跌落到一個硬質表面上后應符合3.1的要求。
5. 指示單元
5.1 分辨力
體溫計指示單元的分辨力應為0.1℃。
5.2 顯示
體溫計顯示器上的數值高度至少為4mm,或通過視覺上的放大效果來達到。
5.3 提示/報警功能
當以下一個或多個數據超過制造商規定的限度時,體溫計應有聲或光的提示/報警信號,或停止提供溫度讀數。
a) 顯示范圍;
b) 電源電壓;
5.4 低電壓提示功能
當電壓低于2.4V±0.2V時,體溫計應開始出現低電壓符號。
5.5 模式
a) 體溫計應具備額溫模式。
b) 以校準為目的的校準模式應通過直接將體溫計設置到該模式。
6. 安全要求
額溫計應符合GB 9706.1-2007的要求。
7. 清潔和消毒
額溫計可以被清潔、消毒,則應提供有關這些程序的指導說明。對額溫計進行清潔,消毒之后,額溫計應符合3.1規定的要求,并且其外殼上的標志不應受到影響。
8. 自檢功能
額溫計應具有自動化的自我檢測順序,并應在有關資料中提供例如如何操作自我檢測順序的相關信息。正常的操作應通過正確的顯示表現出來。
9. 自動關機功能
額溫計應具有自動關機功能。
10 記憶功能
額溫計應具有存儲和查看測量結果的功能。
11. 技術/使用說明書
體溫計產品技術/使用說明書至少應包括下列內容:
11.1 溫度顯示范圍,溫度單位,最大允許誤差,正常工作和貯存條件。
11.2 被測對象的人群、身體部位和額溫計的臨床準確度或臨床偏差。
11.3 校準模式和估算模式的轉換方法,并列出對應部位偏移和用于計算估算模式的相應統計方法
12. 環境試驗要求
氣候環境試驗應符合表1的要求,機械環境試驗應符合GB/T14710-2009中II
組的要求。運輸試驗應符合GB/T14710-2009中第4章的要求,電源電壓適應能力應符合GB/T 14710-2009中第5章的規定。
表1 環境試驗項目,試驗條件,試驗要求及檢測項目
試驗項目及試驗條件 | 試驗要求 | 檢測項目 | 試驗狀態 | |||||
箱內試驗時間h | 箱內持續時間h | 箱內恢復時間h | 中間檢驗 | 最后 檢驗 | 電源電壓適應能力試驗 | |||
d.c.2.7V | d.c.3.15V | |||||||
常溫試驗 | —— | —— | —— | —— | 全性能 | —— | —— | —— |
額定工作低溫試驗16℃ | 1 | —— | —— | —— | 2.2 2.3.1 | √ | —— | 通電 |
低溫貯存試驗-20℃ | 4 | —— | 4 | —— | —— | —— | —— | |
額定工作高溫試驗35℃ | 1 | 4 | —— | 2.2 2.3.1 | —— | √ | 通電 | |
高溫貯存試驗55℃ | 4 | —— | 4 | —— | —— | —— | —— | |
額定工作濕熱試驗35℃ 85% | 4 | —— | —— | —— | —— | —— | 通電 | |
濕熱貯存試驗40℃ 93% | 48 | —— | 24 | —— | —— | —— | —— | |
振動試驗碰撞試驗 | 一個試驗方向,正常工作位置 | —— | 2.1 | —— | —— | —— | ||
運輸試驗 | 正常包裝狀態 | — | 全性能(2.6、2.11除外) | —— | —— | —— | ||
13. 電磁兼容要求
額溫計應符合YY 0505-2012的要求。
五、額溫計主要參考技術標準或規范
額溫計沒有專標,但可以參考國標:“GB/T 21417.1-2008醫用紅外體溫計 第1部分:耳腔式”,結合“耳腔式醫用紅外體溫計注冊技術審查指導原則”確定其技術性能指標。
標準編號 | 標準名稱 |
GB 9706.1—2007 | 醫用電氣設備第一部分:安全通用要求 |
GB/T 14710—2009 | 醫用電器環境要求及試驗方法 |
GB 15980—1995 | 一次性使用醫療用品衛生標準 |
GB/T16886.1—2011 | 醫療器械生物學評價第1部分:風險管理過程中的評價與試驗 |
GB/T 16886.5—2017 | 醫療器械生物學評價第5部分:體外細胞毒性試驗 |
GB/T 16886.7—2015 | 醫療器械生物學評價第7部分:環氧乙烷滅菌殘留量 |
GB/T 16886.10—2017 | 醫療器械生物學評價第10部分:刺激與遲發型超敏反應試驗 |
YY/T 0466.1—2009 | 醫療器械用于醫療器械標簽、標記和提供信息的符號第1部分:通用要求 |
YY 0505—2012 | 醫用電氣設備第1—2部分:安全通用要求并列標準:電磁兼容要求和試驗 |
GB/T21417.1—2008 | 醫用紅外體溫計第1部分:耳腔式 |
YY/T 0664—2008 | 醫療器械軟件生存周期過程 |
YY/T 0708—2009 | 醫用電氣設備第1—4部分:安全通用要求并列標準:可編程醫用電氣系統 |
六、額溫計注冊審批時限
國產額溫計產品在一般審批情況下,其注冊審批周期為80工作日(不含補正過程):
- 技術審評:60個工作日,發補后再60個工作日;
- 行政審批:20個工作日。
