近日,藥監局發布了2017年國家醫療器械不良事件監測年度報告,對2017年醫療器械不良事件監測工作進行了匯總,統計了2017年不良事件報告數量,并對報告的來源、醫療器械管理類別、產品類別等進行分析。
全國醫療器械不良事件報告總體情況
2017年,國家藥品不良反應監測中心共收到《醫療器械不良事件報告表》376,157份,比2016年增長了6.49%。其中,死亡可疑不良事件報告211份,嚴重傷害可疑不良事件報告57,754份,百萬人口平均醫療器械不良事件報告數為282份。
截至2017年12月31日,在“全國醫療器械不良事件監測系統”中注冊的基層用戶數量較2016年有所增長,共注冊用戶253,250家。其中,醫療器械生產企業11,898家,占注冊基層用戶總數的4.70%;經營企業128,625家,占注冊基層用戶的50.79%;使用單位112,727家,占注冊基層用戶的44.51%
2017年醫療器械不良事件報告統計分析
(一)按報告來源統計分析
2017年,全國上報的醫療器械不良事件報告中,使用單位上報326622份,占總報告數的86.83%;生產企業上報8655份,占總報告數的2.30%;經營企業上報40754份,占總報告數的10.83%;還有120份報告來自個人,占總報告數的0.03%;此外還有6份報告來源不詳(圖1)。
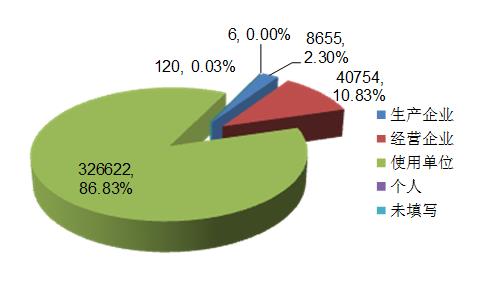
圖1 2017年醫療器械不良事件報告來源情況
(二)按事件傷害程度統計分析
2017年,全國上報的醫療器械不良事件報告中,事件傷害為死亡的報告共211份,占總報告數的0.06%;事件為嚴重傷害的報告共57754份,占總報告數的15.35%;事件傷害為其他的報告共318192份,占總報告數的84.59%(圖2)。2017年,各類傷害程度的報告所占比例與2016年基本一致。
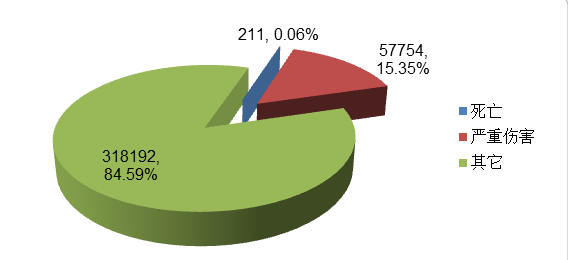
圖2 2017年醫療器械不良事件報告事件傷害程度情況
(三)按醫療器械管理類別統計分析
2017年,全國上報的醫療器械不良事件報告中,涉及Ⅲ類醫療器械的報告154,192份,占總報告數的40.99%;涉及Ⅱ類醫療器械的報告181,175份,占總報告數的48.16%;涉及Ⅰ類醫療器械的報告25,555份,占總報告數的6.79%;部分報告涉及的器械管理類別不詳,共15,235份,占總報告數的4.05%。數據顯示,涉及Ⅲ類和Ⅱ類醫療器械的報告占絕大多數,這與醫療器械風險程度高低相吻合(圖3)。
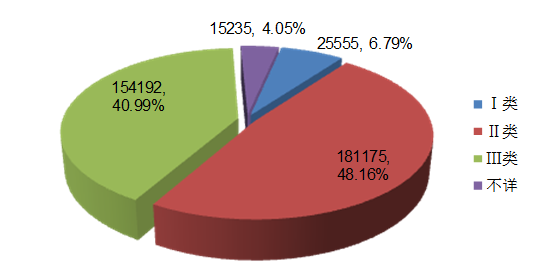
圖3 2017年醫療器械不良事件報告涉及產品管理類別情況
(四)按醫療器械產品名稱統計分析
2017年,全國上報的醫療器械不良事件報告中,報告數量排名前十位的無源醫療器械分別為一次性使用輸液器、一次性使用無菌注射器、靜脈留置針、宮內節育器、導尿包、角膜接觸鏡、玻璃體溫計、導尿管、醫用輸液貼和一次性使用心電電極,占總報告數的35.89%,詳見表1。
排名 | 產品名稱 | 報告數 | 占報告總數的百分比 |
1 | 一次性使用輸液器 | 43538 | 11.57% |
2 | 一次性使用無菌注射器 | 31736 | 8.44% |
3 | 靜脈留置針 | 14757 | 3.92% |
4 | 宮內節育器 | 12441 | 3.31% |
5 | 導尿包 | 7348 | 1.95% |
6 | 角膜接觸鏡 | 7266 | 1.93% |
7 | 玻璃體溫計 | 6786 | 1.80% |
8 | 導尿管 | 4756 | 1.26% |
9 | 醫用輸液貼 | 3772 | 1.00% |
10 | 一次性使用心電電極 | 2662 | 0.71% |
合計 | 135062 | 35.89% |
表1 報告數量排名前十位的無源醫療器械
2017年,全國上報的醫療器械不良事件報告中,報告數量排名前十位的有源醫療器械分別為病人監護儀、輸液泵和注射泵、心電圖機、電子血壓計、血液透析機、呼吸機、生化分析儀、特定電磁波治療機、嬰兒培養箱、血糖儀,占總報告數的9.78%,詳見表2。
編號 | 產品名稱 | 報告數 | 占報告總數的百分比 |
1 | 病人監護儀 | 12917 | 3.43% |
2 | 輸液泵和注射泵 | 7947 | 2.11% |
3 | 心電圖機 | 3109 | 0.83% |
4 | 電子血壓計 | 3105 | 0.83% |
5 | 血液透析機 | 2423 | 0.64% |
6 | 呼吸機 | 2328 | 0.62% |
7 | 生化分析儀 | 1383 | 0.37% |
8 | 特定電磁波治療機 | 1355 | 0.36% |
9 | 嬰兒培養箱 | 1167 | 0.31% |
10 | 血糖儀 | 1063 | 0.28% |
合計 | 36797 | 9.78% |
表2 報告數量排名前十位的有源醫療器械
(五)按涉及實際使用場所統計分析
2017年,全國上報的醫療器械不良事件報告中,使用場所為“醫療機構”的報告311,860份,占82.91%;使用場所為“家庭”的報告33,460份,占8.90%;使用場所為“其他”的報告6,853份,占1.82%;使用場所未填寫的報告23,984份,占6.38%(圖4)。使用場所的復雜性是分析不良事件發生原因時需要考量的因素之一。
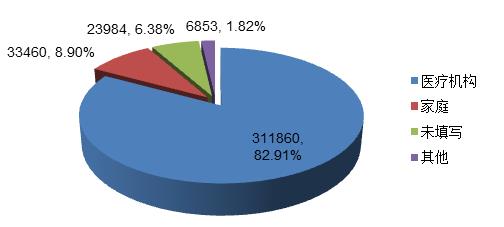
圖4 2017年醫療器械不良事件報告涉及實際使用場所情況
醫療器械警戒快訊發布情況
2017年,國家藥品不良反應監測中心共發布6期《醫療器械警戒快訊》,包括生物可吸收性血管支架系統、除顫/監護系統、胰島素筆式注射器、植入式心臟復律除顫器等32條產品安全性信息。
