活動背景
自2014年6月1日新版《醫療器械監督管理條例》實施以來,與之配套的管理辦法及規范也于近年陸續修訂并發布實施,醫療器械全生命周期監管體系已經形成,企業在產品設計開發、生產、注冊、臨床試驗、經營、使用等過程需在新的醫療器械監管法規下運營。在這一背景下,如何全面滿足更新迅速的最新要求、如何合理規劃,短時間、低成本的做好法規應對工作,是廣大醫療器械企業面臨的問題。“建立最嚴謹的標準、實行最嚴格的監管、實施最嚴厲的處罰、實現最嚴肅的問責”,2015年以來,醫療器械領域的‘四個最嚴’監管行動在全國上下全力推進。注冊階段,質量體系每家必查并拓展至海外企業;臨床試驗成重災區,數據造假已入刑法;今年4月,上海企業非法經營罰沒百萬...... 風險控制,已然是企業在法規應對工作中的重中之重!
值此瑞旭成立十年之際,為回饋廣大客戶對我司一如既往的支持與厚愛,杭州瑞旭產品技術有限公司特舉辦“醫療器械合規現場咨詢活動”。為企業在醫療器械研發、生產、注冊、檢測、臨床、質量管理體系實施、經營過程合規提供合理操作建議,為企業零風險、低成本合規運營保駕護航。
活動形式:
企業預約報名,現場一對一免費咨詢. 我們是您最專業的法規顧問!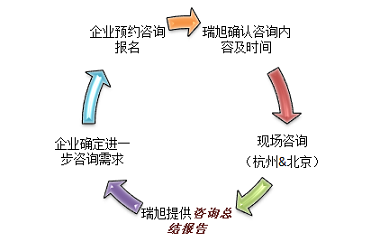
活動時間
每周五下午(2017年5-6月)活動地點
地點一:杭州市濱江區秋溢路288號東冠高新科技園1號樓11層 會議室地點二:北京市西城區宣武門西大街28號大成廣場7門1111室
聯系方式
杭州:張先生0571- 87206527 zjj@cirs-group.com北京:徐女士 010-63984062 xuyn@cirs-group.com
預約報名方式:
1.關注微信公眾號,回復“現場咨詢”獲得報名方式
2. 掃下方二維碼直接報名

3. 如有任何問題,請咨詢我們 0571-87206527
咨詢內容(舉例)
- 新設立醫療器械公司如何合規及準備產品注冊申報工作?
- 和我們公司及產品息息相關的最新規定有哪些?
- 醫療器械產品注冊申報及生產許可流程?
- 如何規劃醫療器械項目?
- 醫療器械注冊單元如何確定?
- 醫療器械管理類別及屬性如何確定?
- 醫療器械技術要求如何編制?
- 醫療器械注冊申報成本預算如何確定?
- 醫療器械設計開發過程如何準備注冊申報工作?
- 醫療器械生產質量管理體系如何建立并運行?
- 醫療器械注冊檢測委托流程及策略
- 醫療器械臨床試驗流程及策略
- 醫療器械臨床試驗如何進行質量控制?
- 醫療器械臨床試驗如何規劃時間、節約成本?
- 醫療器械注冊證如何變更、延續?
- 醫療器械生產許可證申辦流程及要求?
- 醫療器械經營許可證申辦流程及要求?
- 創新醫療器械、優先審批醫療器械申辦流程及要求?
